
Menos é mais
A Odontologia enriquecida por nanomateriais pode ganhar na estética, na durabilidade e na eficácia dos produtos, além de contar com melhor cicatrização e com tratamentos mais rápidos
A manipulação dos elementos em escala nanométrica dá outra dimensão ao velho ditado “menos é mais” quando o assunto é nanotecnologia.
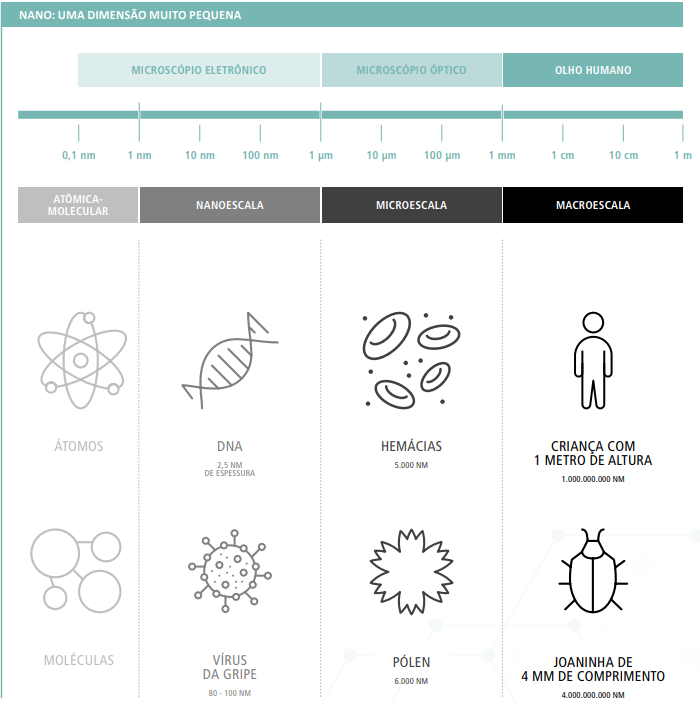
As inovações da nanociência, em que um bilionésimo de algo pode ter um impacto maior e mais eficaz do que esse algo em sua dimensão convencional, alcançam diversas áreas, da eletrônica à biomedicina. Mas vamos por partes, ou melhor, nanopartes.
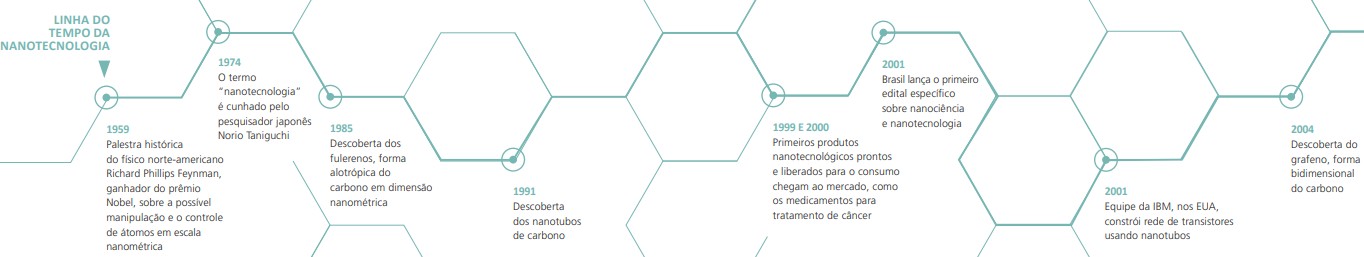
O prefixo “nano” vem do grego, significa “anão” e está relacionado à medida de alguma coisa dividida um bilhão de vezes. Já o termo “nanotecnologia” foi cunhado pelo professor Norio Taniguchi, da Universidade de Ciências de Tóquio, em 1974, e se refere a uma área da tecnologia que manipula a forma e o tamanho da estrutura molecular dos materiais para criar aplicações inovadoras. Entre diversos exemplos está o grafeno, um dos materiais mais finos e resistentes do mundo, composto por uma camada de átomos de carbono. Ele é mais rígido que o aço e mais leve que o alumínio, além de ser flexível, transparente e conduzir calor de forma mais potente que o cobre.
Embora o tema possa parecer de filmes de ficção científica, os nanomateriais já fazem parte do mercado brasileiro desde o início dos anos 2000. A utilização dessas partículas pode variar desde diagnóstico e tratamento de câncer e desenvolvimento de células de painéis solares, até produção de roupas e equipamentos hospitalares com propriedades bactericidas e aperfeiçoamento de cosméticos (como protetores solares).
Já o mercado não é nada microscópico. O Centro Nacional de Pesquisa em Energia e Materiais (CNPEM) estimou que mais de 12 mil empresas de 53 países já haviam empregado nanotecnologia em seus produtos em 2019. Até 2024, é esperado que esse mercado global ultrapasse a marca de US$ 125 bilhões, de acordo com o relatório Global Nanotechnology Market (by Component and Applications) da Research & Markets. E considerando apenas o mercado de plástico antimicrobiano – aplicado a embalagens, setor automotivo, bens de consumo, medicina e saúde, construção e outros –, a estimativa de investimento é de US$ 22,9 bilhões até 2025, segundo a MarketsandMarkets, empresa americana de pesquisa de mercado.

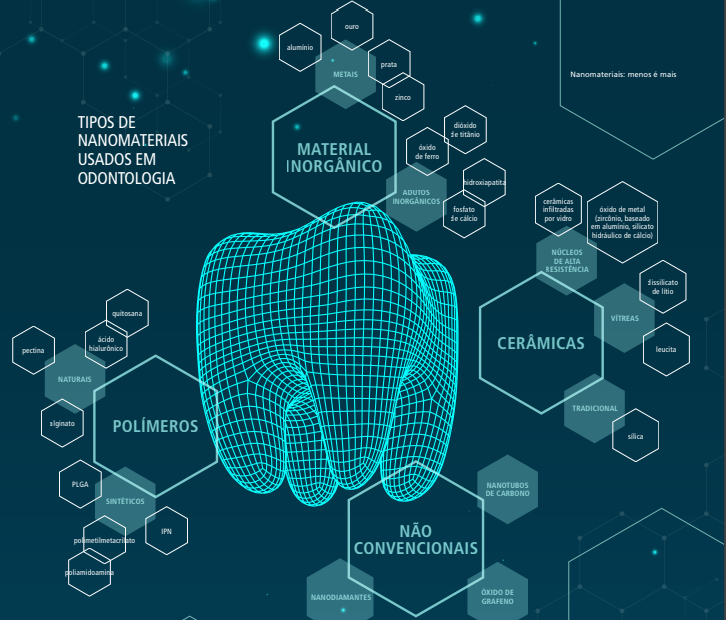
APLICAÇÕES NA ODONTOLOGIA
Os biomateriais dentários são estudados há décadas e podem ser materiais inorgânicos (metais), cerâmicas (carbonos, lentes cerâmicas e vidros) ou polímeros, sintéticos ou naturais (produtos vegetais e animais). Com o surgimento da química ecológica e verde, a demanda por polímeros de origem natural cresceu.
“A Odontologia clínica já tem aplicação de nanotecnologia desde 2003, na área restauradora e de implante. E o Brasil está avançado, é referência em nano aplicada nesta área”, revela o cirurgião-dentista Eduardo Mota, professor do curso de Odontologia da Pontifícia Universidade Católica do Rio Grande do Sul (PUC-RS) e especialista em materiais odontológicos. Para Mota, esses avanços aumentam a sensação de lisura, diminuem o acúmulo bacteriano e proporcionam uma melhora estética. No nicho dos implantes, por exemplo, aceleram o processo de cicatrização, então o paciente conclui seu tratamento com maior rapidez.
Os produtos de nano-Odontologia mais utilizados hoje no mercado incluem nanocompósitos, nanoimpressão, enxaguantes bucais anti-infecciosos e nanopreenchimentos, de acordo com a importante revisão sistemática de estudos intitulada Nanomaterials in Dentistry: Current Applications and Future Scope, publicada recentemente na revista científica Nanomaterials.1 Realizado por cientistas de universidades da Arábia Saudita e da Índia, o artigo abrangeu aproximadamente 160 estudos da área.
Entre os materiais mais pesquisados está a hidroxiapatita, uma forma cristalizada do fosfato de cálcio. “Ela tem propriedades de excelente compatibilidade com o esmalte dentário. Na escala nanométrica, é capaz de preencher e ser incorporada pelas microerosões do esmalte, melhorando sua resistência. Em cremes dentais, mostrou resultados muito superiores aos comuns”, explica o químico Delmárcio Gomes, PhD em Química com ênfase em Nanotecnologia e coordenador da Plataforma EnsiNANO, dedicada ao ensino e à divulgação da nanotecnologia.
PREVENÇÃO
A revisão aborda ainda como nanopartículas metálicas mostram enorme potencial antimicrobiano no tratamento de cáries ou outras doenças dentárias (confira no quadro um exemplo bem-sucedido desse tipo de aplicação feita no Brasil). Os produtos preventivos funcionam de duas maneiras: reduzindo a produção de biofilme ou restaurando o dente danificado por técnicas de remineralização, para inibir o dano adicional à polpa e impedir a degradação do dente. As cáries também podem ser inibidas por meio da prevenção antibacteriana para a cavidade oral.

A literatura sugere que as bactérias são mais propensas a adquirir resistência aos antibióticos convencionais. Portanto, os metais nanoparticulados foram considerados a melhor escolha para a exploração na atividade antimicrobiana. Entre eles estão prata, zinco, níquel, titânio e ouro, que oferece boa biocompatibilidade.
Entre as aplicações, pastas de dente incorporam acetato de zinco e citrato para controlar a formação de placa. Delmárcio cita uma pesquisa que estuda a adição de nanopartículas de prata nas cerdas das escovas. “Já se sabe que a nanoprata tem atividade bactericida. Então a adição dessa prata nanométrica na cerda vai levar a uma redução significativa da doença periodontal”, explica.
O especialista também lembra investigações em desenvolvimento para adicionar fluoreto de cálcio nanoencapsulado a soluções de enxaguante bucal, o que se provou capaz de reduzir significativamente a atividade de cárie e a permeabilidade pela dentina, aumentando a concentração de flúor no fluido oral. “Ele também foi capaz de promover a remineralização de lesões provocadas por cáries, uma inovação que vai trazer resultados muito importantes para a saúde bucal”, completa.
IMPLANTES
A nanotecnologia vem agregando uma maior biocompatibilidade tanto aos implantes como aos materiais de enxertia. “Ela não apenas minimiza a resposta inflamatória do organismo, mas também aumenta a velocidade e a qualidade da regeneração dos tecidos duros e moles, fundamentais para devolver a qualidade funcional a esses pacientes”, explica o cirurgião-dentista Fernando Ferraz, especialista em periodontia pela Faculdade de Odontologia da Universidade de São Paulo (FOUSP), com mais de 20 anos de experiência nas áreas de cirurgia bucal, implantes osseointegrados e regeneração tecidual guiada.
Diversos estudos usam diferentes modificações de superfície para melhorar os principais desafios relacionados a inflamações, osteointegração e processo regenerativo biológico (adsorção de proteínas, adesão, diferenciação e proliferação de células, o que inicia a regeneração do tecido). O revestimento sobre implantes de titânio e zircônia tetragonal, por exemplo, foi explorado para aperfeiçoar propriedades biológicas e mecânicas. Em uma pesquisa2 feita com ratos com osteoporose induzida por ovariectomização, nanopartículas de quitosana de ouro, carregando o gene c-myb, melhoraram a osseointegração de implantes. Além disso, nanocompósitos de sílica também já foram utilizados para aprimorar a resistência mecânica e o crescimento ósseo.
A superfície do implante, por sua vez, pode ser tratada por nanocristais de hidroxiapatita e nanopartículas de cálcio-fósforo para potencializar a regeneração óssea. Por outro ângulo, para superar os problemas de toxicidade e comportamento corrosivo dos implantes à base de metal e cerâmica, têm sido analisados biomateriais derivados de plantas. “No dia a dia, uso implantes dentários com superfície de titânio nanoestruturada, formando um revestimento catalisador cicatricial reabsorvível, que acelera as qualidades biológicas do processo de osseointegração”, diz Ferraz.
Ele também aplica enxerto ósseo com grânulos de hidroxiapatita e beta trifosfato de cálcio, que são convertidos em tecido ósseo devido à estrutura ultraporosa que favorece a fixação celular e antecipa o processo regenerativo. E lembra que, antigamente, os implantes precisavam de um período de até seis meses para receber a carga mastigatória e fazer a osseointegração. Com a nanotecnologia, a adaptação foi acelerada para quatro semanas.
“Em relação aos materiais de enxertia, apesar de o padrão ser o próprio osso do paciente, os biomateriais cada vez mais se apresentam com propriedades osteocondutoras, que possibilitam que o próprio organismo promova a nova formação óssea nos sítios de interesse. Membranas sintéticas de colágeno permitem ainda a devolução de volume de tecidos moles perdidos”, diz.
DEMAIS ESPECIALIDADES
Para Delmárcio, da Plataforma EnsiNANO, outro tópico relevante é a incorporação de nanoesferas com triclosan injetadas, já comprovado cientificamente que promoveu uma redução significativa da inflamação periodontal. Justamente por permitir que o princípio ativo seja liberado lentamente, a cápsula teve uma eficácia muito maior comparada a medicamentos comuns.
O cirurgião-dentista Osmir Batista, professor do departamento de Odontologia Restauradora da Faculdade de Odontologia da Universidade Estadual Paulista (Unesp), concorda. “Presentes há alguns anos, as resinas compostas nanoparticuladas, ou em forma de clusters, têm desempenho mecânico mais otimizado, maior resistência ao desgaste e à fratura. Isso fez aumentar a aplicação desse material e criou soluções para situações que até então só seriam resolvidas com próteses indiretas, com trabalhos mais caros e de mais difícil solução”, conta Batista.

O professor também cita a aplicação de nanotecnologia na cimentação de peças ortodônticas, bem como em adesivos dentinários, o que possibilitou a evolução das lentes de contato, das facetas e das próteses com mínimo desgaste dos dentes. “Na minha área, a gente tem trabalhado com o desenvolvimento de clareamento dental que cause o mínimo desconforto ao paciente e consiga o máximo de resultado estético, com o acréscimo de partículas nanométricas no agente clareador”, diz. Se, normalmente, o produto clareador tem concentração de 35% e é um pouco mais agressivo, é possível trabalhar com clareadores a 6% de peróxido de hidrogênio. “Acaba sendo um material muito menos agressivo, muito mais confortável para o paciente, com o mesmo resultado ou superior ao dos tratamentos tradicionais”.
VANTAGENS E DESAFIOS
As nanopartículas podem melhorar a estética dos materiais, tornando-os mais translúcidos, bem como modificar as propriedades de desgaste, amarelamento e perda de qualidade da superfície.
“As pesquisas que buscam a biocompatibilidade estão avançadas e destacam algumas nanopartículas e materiais que podem ser incorporados a instrumentos cirúrgicos e próteses”, exemplifica Delmárcio.
“A grande vantagem é que, quando você diminui o tamanho das partículas, muda toda a característica inicial do material. Isso faz com que obtenha produtos com um desempenho que, com materiais de tamanho tradicional, não seria possível”, comenta Batista, da Unesp. Aproveitando essa característica e apostando na funcionalização, ele explica por que, nesse caso, o tamanho é essencial. “Como são muito muito pequenos, não há barreiras que os impeçam de acessar qualquer tecido. Eles podem funcionar como mísseis que vão especificamente em células tumorais. Então podem ser ingeridos, por exemplo, cair na corrente sanguínea e só atuar na área de interesse.”

Além desses pontos, outras vantagens do uso dessas partículas envolvem economia de recursos, capacidade de inchaço variável, força flexível e maior rigidez, diagnóstico rápido e preciso, melhor controle sobre a liberação de medicamentos e porosidade controlada, levando a um maior encapsulamento do fármaco e a uma maior regeneração tecidual.
Mas ainda há alguns obstáculos a superar, é claro. “A nanotecnologia é cara, produzir em larga escala ainda é difícil. Ela, então, tem impacto em um grupo da população que não é a base. Um dos desafios é escalonar a produção, reduzir os custos e aumentar o impacto na população em geral”, pontua Mota, da PUC-RS.
Vale destacar que, como são muito pequenos, os nanomateriais envolvem inúmeras questões éticas e regulatórias com relação à toxicidade, ao preconceito do consumidor e também à falta de pesquisas exploratórias em modelos in vitro e in vivo. Segundo a revisão de estudos citada no início da reportagem, por exemplo, os nanotubos de carbono usados em revestimentos dentários apresentaram algumas reações inflamatórias quando em contato com membrana biológica. Além disso, durante a preparação de nanomateriais, entre eles o dióxido de titânio, a exposição por inalação pode causar sintomas tóxicos nos pulmões.
Já as partículas de hidroxiapatita, quando empregadas em uma obturação dentária, ligam-se às proteínas do sangue, formando um complexo que é morto pelos macrófagos e depois transferido para os principais órgãos vasculares, como o pulmão e o baço, com possíveis reações tóxicas. Efeitos genotóxicos e imunotóxicos também foram exibidos por nanomateriais de sílica e zircônio, principalmente devido a espécies reativas de oxigênio. Para o professor Eduardo Mota, porém, é preciso dar um voto de confiança aos órgãos de saúde. “Todos os produtos que são desenvolvidos passam por estágios de testes e de pesquisa. Temos a Anvisa, e os Estados Unidos têm a FDA. Então, se for tóxico, não vai para o mercado”, conclui Mota.
DE OLHO NO FUTURO
Por muito tempo, as pesquisas odontológicas focaram apenas em nanocompósitos. Com o tempo, a tendência mudou para outros tópicos, como as nanoenzimas, ou seja, nanopartículas inorgânicas, com propriedades semelhantes às das enzimas. São menos dispendiosas, fáceis de sintetizar, mais estáveis e altamente eficientes em comparação com os seus homólogos naturais. Já foram desenvolvidas nanoenzimas de DNA para biossensorizar a presença de bactérias dentárias, assim como inibir especificamente o Streptococcus mutans patogênico.
Na área de impressão 3-D, foi possível a fabricação de um nanocompósito de policaprolactona e hidroxiapatita liberador de vancomicina (um antibiótico) usando esse tipo de modelagem tridimensional.3 Os scaffolds (enxertos ósseos) mostraram maior resistência e liberação sustentada do fármaco por até 14 dias, o que pode auxiliar na regeneração tecidual com atividade antimicrobiana. No entanto, apesar do sucesso na síntese de scaffolds de regeneração óssea, poucas pesquisas foram feitas no domínio da nano-Odontologia, o que a torna uma área potencial para estudos futuros.
Outra frente com potencial é o desenvolvimento de nanorrobôs para realizar penetrações programadas, limpar o tecido cariado e colocar compósitos no local necessário com o auxílio da tecnologia de preenchimento 3-D. Nanobots magnéticos já foram utilizados em operações de canal. Esses nanorrobôs podem ir mais fundo na dentina, o que é difícil usando métodos convencionais. Em uma simulação para demonstrar uma restauração dentária (4), em 2015, o resultado foi o aumento da velocidade em oito vezes.
Como se pode perceber, diversas pesquisas inovadoras são realizadas há anos, mas os resultados levam algum tempo para chegar aos consultórios. Isso se deve, principalmente, às questões regulatórias e de biossegurança relacionadas ao tema. Por essa razão, os cientistas acreditam que o verdadeiro potencial da nano-Odontologia ainda está longe de ser alcançado.
REVOLUÇÃO NA ÁREA DE MEDICAMENTOS
Os avanços da nanotecnologia aplicada aos remédios impactaram diversas especialidades médicas, como tratamentos de reposição hormonal e enzimática, contra câncer e doenças incapacitantes. As principais inovações estão ligadas ao direcionamento, transporte e liberação dos fármacos no corpo humano — que se tornam mais flexíveis, personalizados e assertivos com o auxílio das nanopartículas. Isso porque a liberação pode ser feita de forma mais controlada, lenta e continuamente. Um dos mecanismos que permitem que isso aconteça é o encapsulamento por meio de nanoestruturas, que são degradadas aos poucos.
Além disso, o transporte das substâncias ao tecido ou órgão desejado pode aumentar a eficiência dos tratamentos.
Saiba mais:
- Sreenivasalu PKP, Dora CP, Swami R, Jasthi VC, Shiroorkar PN, Nagaraja S, Asdaq SMB, Anwer MK. Nanomaterials in dentistry: current applications and future scope. Nanomaterials. 2022;12(10):1676. https://doi.org/10.3390/nano12101676.
- Takanche JS, Kim JE, Kim JS, Lee MH, Jeon JG, Park IS, Yi HK. Chitosan-gold nanoparticles mediated gene delivery of c-myb facilitates osseointegration of dental implants in ovariectomized rat. Artif Cells Nanomed Biotechnol. 2018;46(S3):S807-17. doi: 10.1080/21691401.2018.1513940. PMID: 30307328.
- Chou PY, Chou YC, Lai YH, Lin YT, Lu CJ, Liu SJ. Fabrication of drug-eluting nano- -hydroxylapatite filled polycaprolactone nanocomposites using solution-extrusion 3D printing technique. Polymers (Basel). 2021 Jan 20;13(3):318. doi: 10.3390/ polym13030318. PMID: 33498261.
- Razavi M, Talebi HA, Zareinejad M, Dehghan MR. A GPU-implemented physics- -based haptic simulator of tooth drilling. Int J Med Robot. 2015;11(4):476-85. doi: 10.1002/rcs.1635. PMID: 25582358.
